Carbonsäure Essigsäure und Essigherstellung
Von: Christopher Müller, Isabel Puchinger, Tom Fleckenstein
Stand: 20.07.2021 |Bildnachweis
Schau dir zunächst das Video auf die folgenden Fragen hin an:
- Wo kommt Essigsäure vor und welche Funktionen hat sie?
- Was ist der entscheidende chemische Unterschied bei der Entstehung von Essigsäure und bei der Produktion von Wein?
- Welche Stoffe entstehen bei der schrittweisen Oxidation von Ethanol?
- Welche Oxidationszahlen liegen in den Atomen von Ethanol, Ethanal und Ethansäure vor?
Weiter unten findest du im Lerncheck die Antworten zu den Fragen und vertiefende Informationen.
Frage
Wo kommt Essigsäure vor und welche Funktionen hat sie?
Antwort
Essigsäure zum Konservieren und als Geschmackstoff in Lebensmitteln. Essigsäure als unerwünschtes Reaktionsprodukt von undichten Weinfässern.
Frage
Was ist der entscheidende chemische Unterschied bei der Entstehung von Essigsäure und bei der Produktion von Wein?
Antwort
Damit Essigsäure entsteht, muss Sauerstoff vorhanden sein. Bei Wein darf kein Sauerstoff vorhanden sein.
Frage
Welche Stoffe entstehen bei der schrittweisen Oxidation von Ethanol?
Antwort
Aus Ethanol entsteht erst Ethanal und dann Ethansäure.
Frage
Welche Oxidationszahlen liegen in den Atomen von Ethanol, Ethanal und Ethansäure vor?
Antwort
Entscheidend ist das Kohlenstoffatom, mit dem die funktionelle Gruppe verbunden ist. Beim Ethanol hat dies die Oxidationszahl -I, beim Ethanal +I und bei der Ethansäure +III.
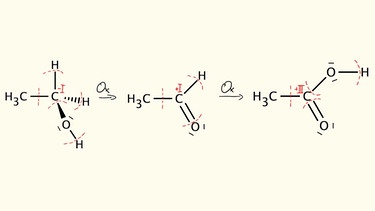
Auch bei organischen Verbindungen finden Redoxreaktionen statt. Hierbei verändern sich die funktionellen Gruppen. Bei der Oxidation von Alkoholen lässt sich das gut nachvollziehen.
So wird beispielsweise ein Ethanolmolekül schrittweise erst zu einem Ethanalmolekül oxidiert und dieses weiter zu einem Ethansäuremolekül.
Den entscheidenden Hinweis liefern die Oxidationszahlen. So hat das Kohlenstoffatom im Ethanmolekül die Oxidationszahl -I, im Ethanalmolekül die Oxidationszahl +I und im Ethansäuremolekül die Oxidationszahl +III.
Redoxreaktionen sind wesentliche Reaktionstypen in der Chemie. Sie laufen nach einem stets gleichen Mechanismus ab. Es findet eine Übertragung von Elektronen statt. Ein Teilchen gibt Elektronen ab und eines nimmt Elektronen auf. Diese beiden Schritte betrachtet man in zwei voneinander getrennten Teilgleichungen.
Teilgleichung 1: Oxidation: Teilchen, das Elektronen abgibt
Teilgleichung 2: Reduktion: Teilchen, das Elektronen aufnimmt
Ein typisches einfaches Beispiel ist die Reaktion von Magnesium (Mg) mit dem Sauerstoff (O2) in der Luft.
Hierbei gibt ein Magnesiumatom zwei Elektronen ab und wird so zu einem zweifach positiv geladenen Magnesium-Kationen oxidiert.
Teilgleichung 1 Oxidation:
Mg —> Mg2+ + 2e-
Gleichzeitig geben beide Sauerstoffatome eines Sauerstoffmoleküls jeweils zwei Elektronen ab (also insgesamt 4 Elektronen) und werden so zu zwei Oxid-Anionen reduziert.
Teilgleichung 2 Reduktion:
O2 + 4e- —> 2 O2-
Um die beiden Teilgleichungen zusammenzufassen, muss nun noch ausgeglichen werden. Natürlich muss die Anzahl der Elektronen, die abgeben und aufgenommen werden, übereinstimmen. In diesem Beispiel wird Teilgleichung 1 also multipliziert mit 2:
Teilgleichung 1 Oxidation:
2 Mg —> 2 Mg2+ + 4e-
Die komplette Reaktionsgleichung erhält man nun, wenn man von beiden Teilgleichungen die Teilchen vor dem Reaktionspfeil und die Teilchen nach dem Reaktionspfeil zusammenträgt und anschließend wenn möglich kürzt:
2 Mg + O2 + 4e- —> Mg2+ + 2 O2- + 4e-
2 Mg + O2 —> MgO2
Nun lässt sich auch erklären, dass aus zwei Elementen der neue Stoff Magnesiumoxid entsteht. Ein Salz, das auf Teilchenebene aus Magnesiumkationen und Oxidationen besteht.
Oxidationszahlen sind ein Konzept, um herauszufinden, welches Teilchen Elektronen abgibt und damit oxidiert wird und welches Teilchen Elektronen aufnimmt und damit reduziert wird.
Es sind im Prinzip "gedachte Ladungen", die sich für jedes Teilchen bestimmen lassen.
In organischen Verbindungen werden sämtliche Bindungselektronen immer dem Atom zugerechnet, das stärker Elektronegativ ist (rote gestrichelte Linien). Anschließend addiert man die Elektronen eines jeweiligen Atoms (blaue Zahlen) und vergleicht diese Zahl mit der Anzahl an Valenzelektronen. Sofern einem Atom mehr Elektronen zugerechnet werden so erhält es eine entsprechende negative Oxidationszahl. Bei weniger Elektronen eine entsprechend höhere Oxidationszahl (rote Zahlen).
Auch in der Natur findet eine Oxidation von Ethanol über Acetaldehyd als Zwischenstufe zur Essigsäure statt. Schon in der Antike war diese chemische Reaktion bekannt und wurde benutzt, um aus Wein Essig herzustellen (vgl. engl. vinegar = Essig von frz. vin aigre = saurer Wein). Vermutlich wurde dieser Prozess wie auch die alkoholische Gärung eher zufällig entdeckt. Lässt man Wein nämlich über längere Zeit offen stehen, siedeln auf der Oberfläche des Weins von selbst Essigsäurebakterien an und oxidieren mit Hilfe des Luftsauerstoffs den im Wein enthaltenen Alkohol zu Essigsäure.
Diese traditionelle Methode der Essigherstellung ist zeitaufwändig und fehleranfällig. Wenn sich statt Essigsäurebakterien zum Beispiel Schimmelpilze ansiedeln und überhand nehmen, bildet sich kein Essig und der Wein verdirbt. Bei mangelnder Sauerstoffzufuhr können die Essigsäurebakterien das Ethanol nur unvollständig oxidieren, es sammelt sich das giftige und stechend riechende Acetaldehyd an, der Essigsäuregehalt bleibt niedrig und der Essig ist für den menschlichen Genuss unbrauchbar. Auch zu kühles oder zu heißes Wetter kann das Wachstum der Essigsäurebakterien hemmen und die Essigproduktion verlangsamen oder ganz verhindern.
Moderne Essigherstellung
Moderne Verfahren zur Essigerzeugung überlassen daher nichts dem Zufall. Der Wein wird in großen Reaktoren gezielt mit Essigsäurebakterien geimpft, konstant auf einer für die Essigsäurebakterien optimalen Temperatur gehalten und durch Düsen ständig mit Sauerstoff versorgt. Die vollständige Umsetzung des Ethanol zu Essigsäure, die bei traditionellen Verfahren mehrere Monate dauert, kann dadurch auf wenige Tage verkürzt werden.
Essig kann aus Wein oder aus anderen alkohohaltigen bzw. zu Alkohol vergärbaren Ausgangsprodukten hergestellt werden. Apfelessig wird zum Beispiel aus Apfelmost, Reisessig aus Reiswein und Branntweinessig aus verdünntem Agraralkohol (zum Beispiel aus Getreide oder Kartoffeln) hergestellt.
Sonderfall Balsamico-Essig
Der berühmteste und teuerste Essig – ein 100ml Fläschchen kann durchaus über 100 € kosten – ist der Balsamico-Essig. Er wird nach einem traditionellen Verfahren aus süßem Wein hergestellt. Durch mindestens 12 Jahre lange Lagerung in Fässern aus verschiedenen Holzarten erhält er eine dickflüssige Konsistenz und ein komplexes Aroma.
Zusatzwissen: Essigsäure in der chemischen Industrie
Essigsäure wird nicht nur für Lebensmittel verwendet, sondern ist auch ein wichtiger Grundstoff für die chemische Industrie. Industriell wird Essigsäure zum größten Teil nicht aus Ethanol, sondern nach dem Monsanto- oder dem neueren Cativa-Verfahren aus Methanol und Kohlenmonoxid hergestellt. Die beiden Verfahren unterscheiden sich vor allem durch den für die Reaktion verwendeten Katalysator.
Die schwach sauren Eigenschaften der Essigsäure nutzt man als
- Geschmackskomponente (Senf, Gurken, Sushi)
- Konservierungsmittel (hält Schimmel und Bakterien fern)
- Entkalker und Badreiniger (Reaktion mit Carbonaten)
- Fotografie (Stoppbad neutralisiert basische Entwickler)
- Essigsäure-Acetat-Puffer (Pufferbereich im Sauren)
Schon die alten Römer nutzten sauren Wein seines erfrischenden Geschmacks wegen als alkoholarmes Erfrischungsgetränk. Auch die Bibel erwähnt Essig als Durststiller, der Jesus am Kreuz gereicht wird (Mk 15,36). Schon früh wurde Essig auch zum Einlegen von Gemüse oder Fleisch verwendet, da im sauren Milieu viele Schimmelpilze und Bakterien nicht lebensfähig sind.
Aber Essig schmeckt nicht nur sauer, sondern ist auch im chemischen Sinn (nach Brønsted) eine Säure.